7月1日,國(guó)際學(xué)術(shù)期刊Nature Communications在線發(fā)表了中國(guó)科學(xué)院分子細(xì)胞科學(xué)卓越創(chuàng)新中心(生物化學(xué)與細(xì)胞生物學(xué)研究所)周小龍研究組聯(lián)合上海交通大學(xué)醫(yī)學(xué)院許泓研究組、湖南大學(xué)王奕蓉研究組的最新研究成果,題為:“Mammalian tRNA acetylation determines translation efficiency and tRNA quality control”。該項(xiàng)工作揭示了哺乳動(dòng)物tRNA 乙酰化修飾對(duì)mRNA翻譯效率及tRNA質(zhì)量控制的新機(jī)制。
tRNA是蛋白質(zhì)合成的關(guān)鍵接頭分子,負(fù)責(zé)將mRNA遺傳信息轉(zhuǎn)換成蛋白質(zhì)氨基酸信息。tRNA含有位置多樣、種類(lèi)豐富的轉(zhuǎn)錄后修飾,精確調(diào)控tRNA的折疊、穩(wěn)定性、密碼子-反密碼子配對(duì)的精準(zhǔn)性、tRNA與相關(guān)蛋白質(zhì)的相互作用等,在遺傳信息傳遞的效率與保真性方面發(fā)揮關(guān)鍵作用。N4-乙酰胞苷(ac4C)于20世紀(jì)60年代率先發(fā)現(xiàn)于tRNA分子上。現(xiàn)已發(fā)現(xiàn)ac4C廣泛存在于原核生物、真核生物與古細(xì)菌tRNA、rRNA及小RNA分子中。此外,在mRNA及病毒RNA中也有ac4C修飾的報(bào)道。在細(xì)菌tRNA中,ac4C只存在于tRNAMet的第34位(ac4C34),其生物學(xué)功能是避免tRNAMet的CAG反密碼子錯(cuò)誤讀取異亮氨酸AUA密碼子,從而確保翻譯的保真性。在古細(xì)菌tRNA中,ac4C存在于多個(gè)tRNA的多個(gè)位置,其豐富伴隨生長(zhǎng)溫度升高而上調(diào),提示其調(diào)節(jié)了熱刺激下的tRNA穩(wěn)定性。在真核生物tRNA中,ac4C特異性地發(fā)生在tRNALeu和tRNASer的C12位(ac4C12),由RNA乙酰轉(zhuǎn)移酶Nat10/Kre33在非酶輔助因子Thumpd1/Tan1的協(xié)同下催化形成。在釀酒酵母中,Tan1基因的缺失會(huì)導(dǎo)致在高溫條件下,tRNASer(CGA)和tRNASer(UGA)被5’-3’核酸外切酶Xrn1/Rat1通過(guò)快速tRNA降解(RTD)途徑選擇性水解。然而,近60年來(lái),ac4C12 在高等真核生物中的生物學(xué)功能尚不清楚。此外,哺乳動(dòng)物細(xì)胞中是否存在RTD途徑也不明確。
在本項(xiàng)研究中,研究人員首先明確Nat10與Thumpd1在細(xì)胞內(nèi)直接相互作用,并基于AlphaFold預(yù)測(cè)的蛋白質(zhì)結(jié)構(gòu)信息,鑒定了Nat10與Thumpd1相互作用的結(jié)構(gòu)域;純化了Thumpd1蛋白質(zhì),證明Thumpd1可以直接結(jié)合底物tRNA;通過(guò)CRISPR-Cas9基因編輯系統(tǒng),構(gòu)建了Thumpd1基因缺失的NIH/3T3細(xì)胞系;Thumpd1的敲除會(huì)導(dǎo)致底物tRNA上的ac4C12修飾喪失,證明Thumpd1是tRNA ac4C12形成必不可少的關(guān)鍵輔助因子;在生理?xiàng)l件下,ac4C12的缺失顯著下調(diào)tRNALeu和tRNASer的氨基酰化水平,該缺陷可以通過(guò)過(guò)表達(dá)相應(yīng)的亮氨酰-tRNA合成酶和絲氨酰-tRNA合成酶加以拯救;通過(guò)翻譯組、RNA-seq等技術(shù)方法,揭示ac4C12的缺失顯著影響全局性翻譯效率,尤其是顯著抑制富含2個(gè)U/A 核苷酸的 Ser/Leu 密碼子的解碼效率;在熱刺激條件下,ac4C12的缺失特異性地導(dǎo)致tRNALeu(CAG)被快速降解;遺傳學(xué)實(shí)驗(yàn)證明,tRNALeu(CAG)的降解是由5’-3’核酸外切酶Xrn1和Xrn2共同介導(dǎo);進(jìn)一步研究表明, Bpnt1及Bpnt2通過(guò)調(diào)控體內(nèi)代謝物3’,5’-二磷酸腺苷(pAp)的水平,進(jìn)而調(diào)節(jié)Xrn1和Xrn2核酸外切酶活性,直接調(diào)控tRNALeu(CAG)的快速水解。研究人員將這條受到精細(xì)調(diào)控的tRNA降解機(jī)制命名為mammalian RTD (mRTD)。
總之,該研究結(jié)果揭示了哺乳動(dòng)物細(xì)胞tRNA ac4C12修飾在生理?xiàng)l件下對(duì)于tRNA氨基酰化以及翻譯效率調(diào)控的新機(jī)制、闡明了ac4C12修飾在熱刺激條件下對(duì)于tRNA穩(wěn)定性的決定性作用、建立了哺乳動(dòng)物細(xì)胞tRNA質(zhì)量控制的新途徑。以上研究結(jié)果進(jìn)一步豐富了人們對(duì)于tRNA修飾多維度調(diào)控mRNA翻譯速率與保真性的功能認(rèn)知。
上海交通大學(xué)劉娜博士、湖南大學(xué)碩士生劉冰雪、分子細(xì)胞卓越中心博士研究生馬春蕊為論文的共同第一作者,分子細(xì)胞卓越中心周小龍研究員、上海交通大學(xué)醫(yī)學(xué)院許泓教授、湖南大學(xué)王奕蓉副教授、上海交通大學(xué)醫(yī)學(xué)院林瑜副研究員為論文共同通訊作者。感謝分子細(xì)胞卓越中心分子生物學(xué)技術(shù)平臺(tái)朱南霖博士、細(xì)胞庫(kù)陳躍磊博士的大力支持。該研究得到了中國(guó)科學(xué)院、科技部、國(guó)家自然科學(xué)基金委、上海市科委的經(jīng)費(fèi)資助。
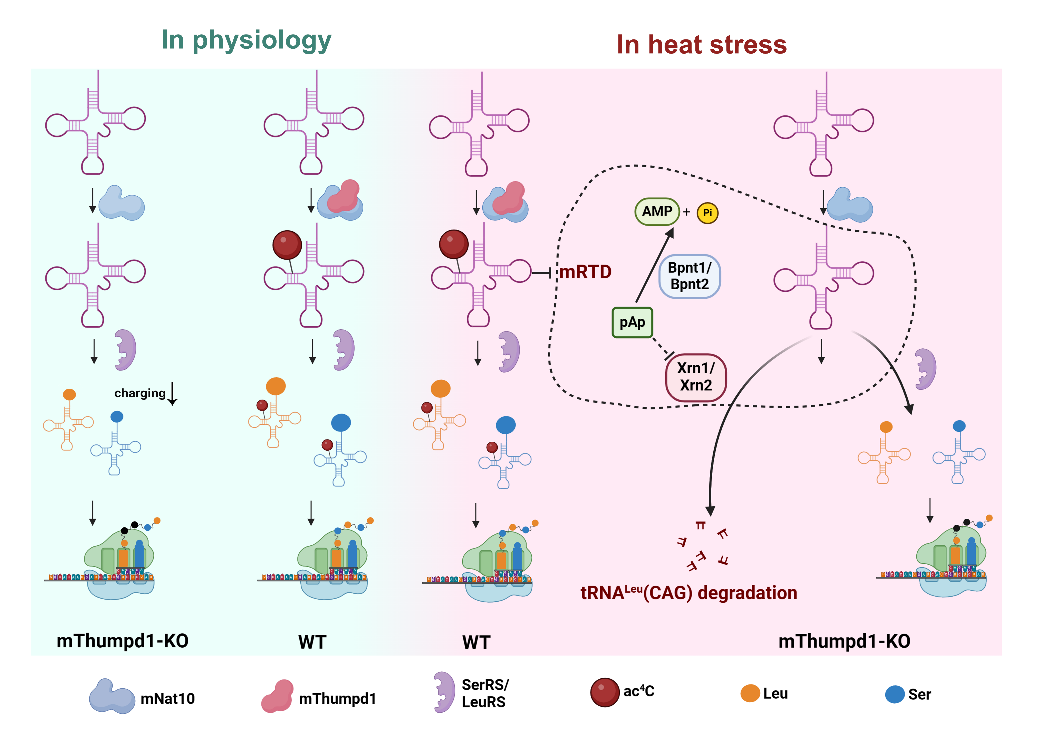
哺乳動(dòng)物tRNA乙酰化修飾調(diào)控翻譯效率及tRNA質(zhì)量控制的新機(jī)制
文章鏈接:https://www.nature.com/articles/s41467-025-60723-3

































